
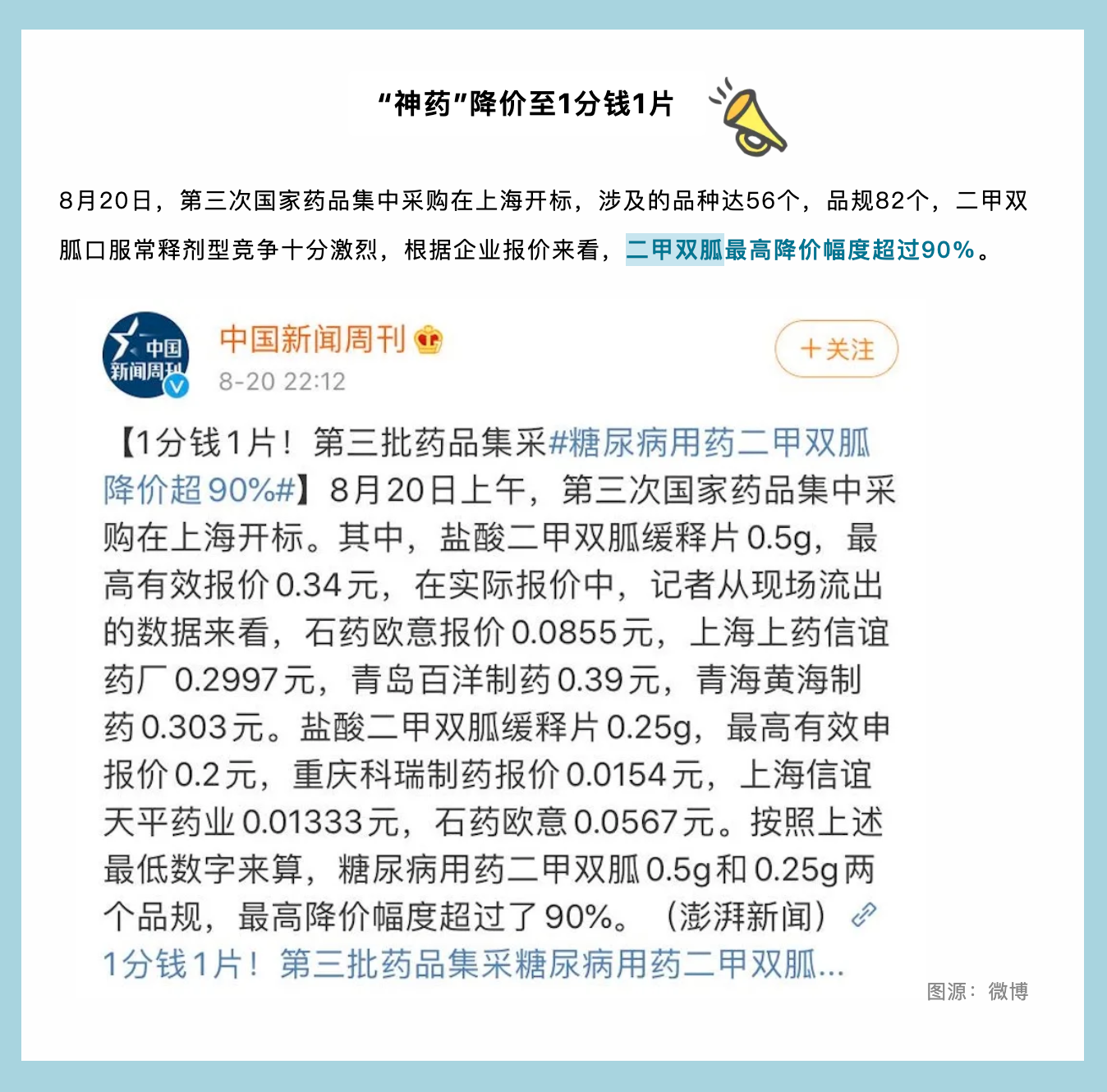
那么问题来了,什么是二甲双胍?


II型糖尿病占糖尿病患者90%以上,全球患病人数高达4.25亿,中国1.16亿,人数居世界第一(2017年)。II型糖尿病患者的患病原因有,胰岛素分泌能力部分丧失,或胰岛素效果差、对胰岛素敏感性降低等,导致血糖升高,最终发展成糖尿病。
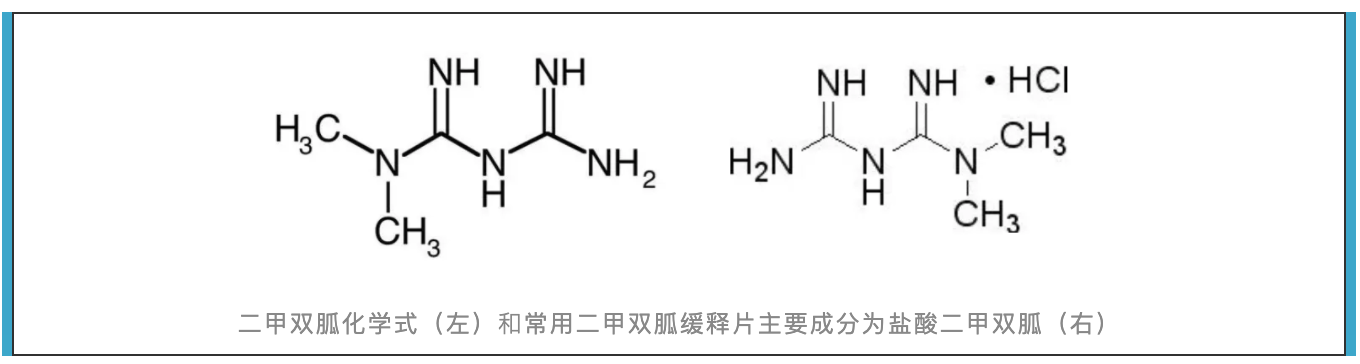
像很多药物一样,二甲双胍也是从天然产物中来。历史可以追溯到中世纪,人们发现山羊豆有催乳、缓解多尿(糖尿病典型症状质疑)的作用。科学家对山羊豆成分进行分析,经过一代代科学家的努力,到19世纪20年代时候,制备了一系列双胍类药物,包括二甲双胍,并验证了其降糖活性。
然而既生瑜何生亮,胰岛素在这一时期被发现,被认为是糖尿病的终结者,在治疗上大显身手,二甲双胍生不逢时,被束之高阁多年。一直到1957年法国糖尿病学家Sterne通过临床试验证实了二甲双胍的降糖作用,并起名“嗜葡萄糖者(glucose eater)”,中文译为“格华止”,才让它重新获批,推向市场。
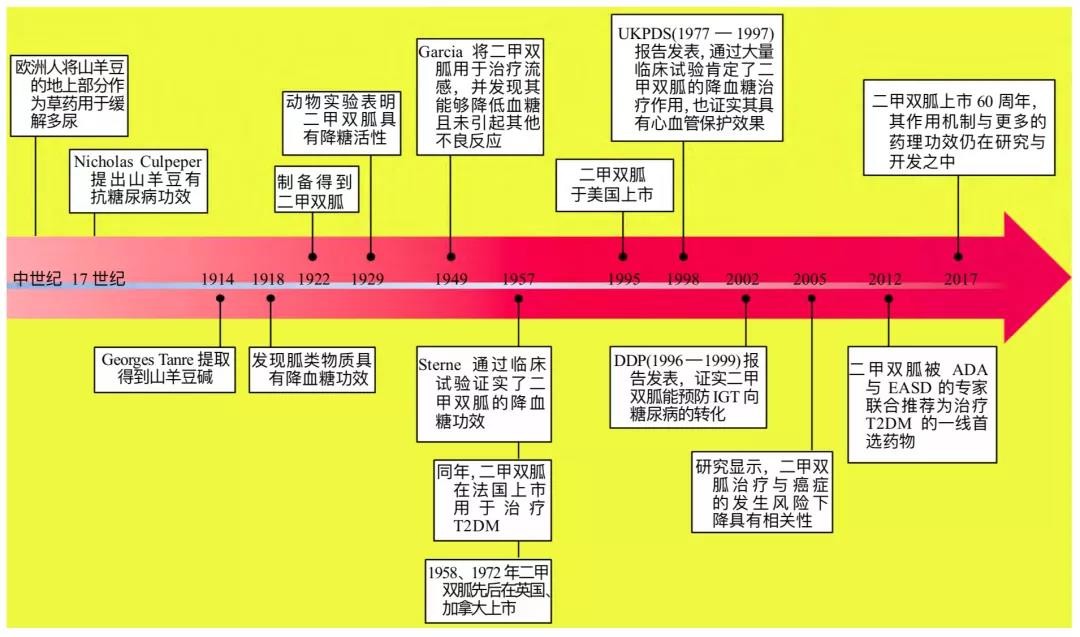
可见即使是一个注定要在临床上大放异彩的神药,年轻时候也要经历不少挫折,简直就是贫寒之子历经挫折、对手打压、朋友背叛后,又遇贵人相助,蛰伏后默默修炼最终彪炳史册的奋斗史。
二甲双胍是如何降低血糖呢?先来看看血糖的来源与去路。胰高血糖素促进来源,使血糖升高;胰岛素控制去路,使血糖降低。
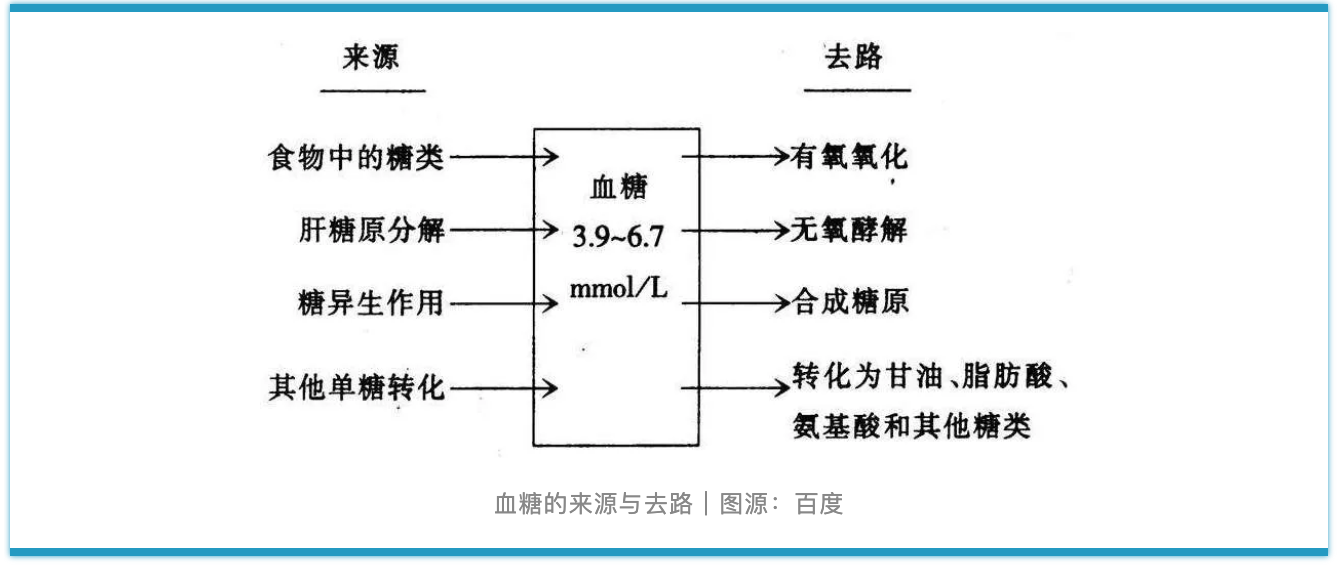
二甲双胍在其中的几个方面都有作用。
1在肝脏中
既可以抑制线粒体的作用,使糖异生减少,且降低胰高血糖素信号;又可以抑制脂类合成,提高胰岛素敏感性。减少了血糖来源,促进了血糖去路,双管齐下,降低血糖。而且它会诱导肝细胞分泌“厌食激素”(GDF15),调节大脑,抑制摄入高脂饮食的欲望。除了肝脏,还调节小肠、结肠和肾脏等全身多处分泌GDF15。自制力不是梦,二甲双胍帮你从脑子开始管住嘴。

2在肠道中
二甲双胍抑制肠壁细胞吸收葡萄糖,降低食物中的糖类来源,还可以提高胰高血糖素样肽-1(GLP-1)的水平,GLP-1是一种激素,可抑制肠道蠕动、降低食欲,促进胰岛素分泌。它还刺激肠道,促进葡萄糖从血液向肠道的运输,直接排出糖。厉害了,二甲双胍!
3在肌肉、脂肪等组织中
二甲双胍也可以降低脂肪酸的水平,提高胰岛素的敏感性,促进组织细胞对血糖的利用,不愧为鼎鼎大名的“噬糖者”。
胰岛素是最直接降低血糖的激素,但使用不当也会引起低血糖、肥胖等,二甲双胍就是它的好帮手。

二甲双胍除了在降血糖中起作用外,还对心血管起保护作用。主要是通过降低血糖、抑制肥胖、非酒精性脂肪肝来降低心血管疾病的风险,还可以调节血管内皮细胞,改善血管舒张和抗凝。
二甲双胍的威力可不限于此。多囊卵巢综合征是一个常见的女性不育的内分泌疾病,发病机制之一就是胰岛素耐受,而二甲双胍可以增加胰岛素敏感性,对治疗很有帮助。
神奇的是二甲双胍还在很多领域有作用,治疗甲状腺疾病有疗效,在神经保护、阿尔茨海默病、自闭症治疗等领域也有一定作用。还能促进小鼠休止期毛囊进入生长期,促进毛发生长。小鼠可以,人类也可以!来自正道的光,照在了饱受秃头困扰的社畜头顶上。
二甲双胍可以在雌激素的作用下,激活大脑的神经干细胞储备,修复大脑损伤。还可以提高老化神经干细胞活力,恢复神经髓鞘再生能力;调节胃干细胞代谢,保护胃功能;还可以逆转非糖尿病患者的心脏损伤。近期很多科学家还开始研究其抗衰老作用,生长激素、脱氢表雄酮与二甲双胍共同服用一年后,平均表观遗传学年龄减少2.5岁,免疫*也有恢复活力的迹象。“懂王”也不过如此了!

流行病学研究显示,II型糖尿病患者肝癌、胰腺癌和*内膜肿瘤的发病率为一般人的2倍,结直肠癌、肾脏肿瘤、膀胱癌和乳腺癌的发病风险为一般人的1.2~1.5倍。使用二甲双胍治疗的II型糖尿病患者,与使用其他药物治疗的患者相比,癌症发病率下降23%。二甲双胍与肿瘤发育中多个通路相互作用,抑制肿瘤生长。

二甲双胍虽然神奇,不过也不是毫无副作用。长期服用二甲双胍会引起维生素B12流失,加速神经*病变,可能会使并发症提前。极少数患者服用二甲双胍会诱发乳酸酸中毒,或者明显的胃肠道不良反应。服用二甲双胍不当会引起低血糖。而且神药的大部分作用还停留在科学研究层面,离真正使用还有距离,千万不要自己随意尝试,切记谨遵医嘱。
###
参考文献:
1. 付炎, 王于方, 吴一兵,等. 天然药物化学史话:二甲双胍60年——山羊豆开启的经典降糖药物[J]. 中草药, 2017, 48(022):4591-4600.
2. Emily A. Day, Rebecca J. Ford, Brennan K. Smith, et al. Metformin-induced increases in GDF15 are important for suppressing appetite and promoting weight loss[J]. Nat*e metabolism, 2019.
3. Xie J, Xia L, Xiang W, et al. Metformin selectively inhibits metastatic colorectal cancer with the KRAS mutation by intracellular accumulation through silencing MATE1[J]. Proceedings of the National Academy of Sciences, 2020.
4. Morita Y, Nogami M, Sakaguchi K, et al. Enhanced Release of Glucose Into the Intraluminal Space of the Intestine Associated With Metformin Treatment as Revealed by [18F]Fluorodeoxyglucose PET-MRI. Diabetes Care. 2020;dc200093. doi:10.2337/dc20-0093
5. Chai M, Jiang M, Vergnes L, et al. Stimulation of Hair Growth by Small Molecules that Activate Autophagy. Cell Rep. 2019;27(12):3413-3421.e3. doi:10.1016/j.celrep.2019.05.070
6. Ruddy R M, Adams K V, Morshead C M. Age-and -dependent effects of metformin on neal prec*sor cells and cognitive recovery in a model of neonatal stroke[J]. Science advances, 2019, 5(9): eaax1912.
7. Fahy GM, Brooke RT, Watson JP, et al. Reversal of epigenetic aging and immunosenescent trends in humans. Aging Cell. 2019;18(6):e13028. doi:10.1111/acel.13028
8. Xie J, Xia L, Xiang W, et al. Metformin selectively inhibits metastatic colorectal cancer with the KRAS mutation by intracellular accumulation through silencing MATE1. Proc Natl Acad Sci U S A. 2020;117(23):13012-13022. doi:10.1073/pnas.1918845117
本文作者:刘思辰,清华大学生命科学学院在读博士生;
鸣谢:复旦大学中山医院药剂科主管药师张捷青为本文提供科学指导。